InFormacion Láser desde el espacio
Septiembre con innovaciones A FUTURA✓
En el vasto horizonte del siglo XXII, la humanidad ha logrado un hito sin precedentes: la conquista del espacio profundo. La exploración espacial ya no es solo una aventura, sino una realidad cotidiana. Las plataformas espaciales flotan como islas tecnológicas en la órbita terrestre y más allá, sirviendo como nodos de conexión entre colonias en Marte, estaciones científicas en Europa y naves de exploración que se adentran en los confines de la galaxia.Estas plataformas, alimentadas por combustibles alternativos basados en la fusión nuclear y el aprovechamiento de materia oscura, han dejado atrás la dependencia de los combustibles fósiles. Los reactores de fusión, encapsulados en campos magnéticos de alta energía, brindan una fuente inagotable de poder, permitiendo a las naves atravesar vastas distancias en fracciones de tiempo antes inimaginables. Además, el aprovechamiento de la antimateria como fuente de energía ha permitido desarrollar motores más eficientes, reduciendo drásticamente los tiempos de viaje interplanetario.La medicina ha dado un salto cuántico con el desarrollo de medicamentos inteligentes, capaces de adaptarse a las necesidades biológicas individuales de cada ser humano, incluso en entornos extraterrestres. Estos fármacos, construidos a nivel nanomolecular, pueden detectar enfermedades en sus fases más tempranas, administrar tratamientos personalizados en tiempo real, y adaptarse a las condiciones ambientales únicas del espacio, como la microgravedad o la radiación cósmica.El futuro es ahora, un tiempo en el que las fronteras de la ciencia, la tecnología y la biología se desdibujan, permitiendo a la humanidad explorar, sanar y prosperar en un universo lleno de posibilidades infinitas.
Estación EspacialLa NASA demostrará comunicaciones láser desde la estación espacial
La Estación Espacial Internacional (EEI) es utilizada por la NASA para llevar a cabo investigaciones y experimentos en areas como biología, tecnología y agricultura, entre otros. Durante más de 20 años, ha sido un hogar para los astronautas y ha proporcionado una plataforma unica para el avance de las capacidades de comunicaciones espaciales.
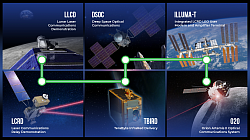
En 2023, la NASA enviará una demostración de tecnología llamada ILLUMA-T a la EEI. ILLUMA-T es un sistema de comunicaciones láser que utiliza luz infrarroja invisible para enviar y recibir información a velocidades de datos más altas. Esto permitirá enviar imágenes y videos a la Tierra de manera más rápida y eficiente.
Además de las velocidades de datos más altas, los sistemas de comunicaciones láser son más livianos y consumen menos energía, lo que los hace ideales para su uso en naves espaciales. ILLUMA-T, que es del tamaño de un refrigerador estándar, se instalará en la estación espacial y se demostrará junto con el sistema de retransmisión láser LCRD de extremo a extremo.
LCRD, que se encuentra en rbita geosincrónica a 22,000 millas de la Tierra, está transmitiendo datos entre dos estaciones terrestres y realizando experimentos para mejorar aún más las capacidades láser de la NASA.
Una vez que ILLUMA-T esté en la estación espacial, enviará datos de alta resolución al LCRD a una velocidad de 1.2 gigabits por segundo, y luego estos datos se enviarán a estaciones terrestres en Hawaii y California. Esta demostración mostrará cómo las comunicaciones láser pueden beneficiar a las misiones en rbita terrestre baja.
ILLUMA-T se lanzará como carga til en una misión de Servicios de Reabastecimiento Comercial de SpaceX para la NASA y se instalará en la Instalación Expuesta del Módulo Experimental Japonés (JEM-EF) de la estación espacial.
https://www.nasa.gov/feature/goddard/2023/nasa-to-demonstrate-laser-communications-from-space-station/
La edición de bases modifica los epítopos de HSC para la inmunoterapia dirigida
Una nueva investigación muestra que la ingeniería de epítopos en células madre y progenitoras hematopoyéticas (HSPC) de donantes utilizadas en trasplantes de médula ósea puede otorgar a los linajes hematopoyéticos resistencia selectiva a los anticuerpos monoclonales o a las células T del receptor de antígeno quimérico (CAR) sin cambiar la regulación o función de las proteínas. Esta táctica hace posible atacar genes esenciales para la supervivencia de la leucemia, incluso si esos genes también se expresan en HSPC. Al hacerlo, se reduce la probabilidad de que el sistema inmunológico se aleje del tumor. También mejorará la seguridad del acondicionamiento no genotóxico y permitirá el tratamiento de la leucemia mieloide aguda resistente o recidivante.
El estudio revisado por pares " La edición de epítopos permite la inmunoterapia dirigida de la leucemia mieloide aguda " proviene del laboratorio de Pietro Genovese, PhD, investigador principal del Programa de Terapia Génica del Centro de Trastornos Sanguíneos y Cáncer Infantil Dana-Farber/Boston y profesor asistente de pediatría. en la Facultad de Medicina de Harvard y se publicó hoy en Nature .
Toxicidad en el objetivo pero fuera del tumor
Dirigirse a antígenos hematopoyéticos prescindibles, células CAR T, anticuerpos biespecíficos y conjugados anticuerpo-fármaco son inmunoterapias adoptivas prometedoras que pueden superar las limitaciones de los tratamientos tradicionales contra el cáncer. Sin embargo, la falta de marcadores restringidos a tumores que puedan usarse de manera segura limita su aplicabilidad a otras neoplasias malignas hematológicas como la leucemia mieloide aguda (LMA).
Dado que la AML y las HSPC normales o las células mieloides diferenciadas comparten la mayoría de los mismos marcadores de superficie, las toxicidades en el objetivo pero fuera del tumor causarían aplasia mieloide y dificultarían que la sangre produzca nuevas células sanguíneas. Puede ser necesario apuntar a múltiples antígenos de superficie debido a la heterogeneidad y flexibilidad de los tumores de AML, lo que plantea la posibilidad de toxicidad superpuesta. Para reducir la probabilidad de erradicación de la AML, actualmente se están desarrollando diversas inmunoterapias para la AML; sin embargo, es probable que su uso se limite al tratamiento puente antes del trasplante alogénico de HSPC (TCMH).
La edición de bases genera receptores sigilosos
El becario postdoctoral Gabriele Casirati, MD, del laboratorio de Genovese, y sus colegas demuestran que los antígenos asociados a tumores presentes en el tejido normal pueden atacarse de forma segura alterando el epítopo que las inmunoterapias adoptivas reconocen en las células sanas, confiriendo resistencia selectiva y creando antígenos artificiales restringidos a leucemia. Este estudio se centró en tres epítopos: la subunidad α del receptor de IL-3 (IL-3RA; también conocido como CD123), KIT (también conocido como CD117) y tirosina quinasa 3 similar a FMS (FLT3; también conocido como CD135). . Estos epítopos se expresan en diferentes etapas del desarrollo hematopoyético normal y más del 75% de los casos de AML los tienen. Su sobreexpresión en las células de AML está relacionada con una tasa de supervivencia general más baja y una mayor incidencia de recaída después del TCMH.
Casirati et al. utilizaron exámenes de biblioteca y mapeo de epítopos para encontrar cambios de aminoácidos que impiden que los anticuerpos monoclonales terapéuticos se unan a FLT3, CD123 y KIT. Luego refinaron una técnica de edición de bases para introducir estas alteraciones en las HSPC CD34+, que aún pueden injertarse y diferenciarse en varios tipos de células durante períodos prolongados. FLT3, CD123 y KIT en HSPC se pueden editar para prevenir la desactivación genética y mantener la expresión, regulación y señalización intracelular de proteínas normales. Es importante destacar que este enfoque permite apuntar a uno o más genes esenciales para la supervivencia de la leucemia, produciendo así una fuerte eficacia antileucemia con baja toxicidad dentro y fuera del tumor.
Después de la terapia con células T con CAR, Casirati y sus colegas verificaron que la hematopoyesis editada con epítopos era resistente y que los xenoinjertos de leucemia mieloide aguda derivados de pacientes se eliminaban al mismo tiempo. Además, demuestran la viabilidad de la ingeniería de epítopos múltiples de HSPC, que puede mejorar la eficacia de las inmunoterapias contra numerosos objetivos sin causar efectos adversos en otras regiones del cuerpo.
Aplicación a través y más allá de las neoplasias malignas hematológicas
Si bien el objetivo principal de este estudio fue mejorar el tratamiento de la AML, la leucemia linfoblástica aguda de células B CD19 recidivante y la leucemia linfoblástica T, que tienen antígenos seguros limitados, pueden beneficiarse del tratamiento de ingeniería de epítopos. Además, se pueden utilizar anticuerpos monoclonales, conjugados anticuerpo-fármaco o activadores de células T biespecíficos con edición de epítopos para aumentar gradualmente el suministro del cuerpo de células autólogas genéticamente modificadas.
Recientemente se ha sugerido un acondicionamiento no genotóxico para enfermedades no malignas utilizando inmunoterapias dirigidas a marcadores específicos de HSPC. Las HSPC editadas con epítopos aumentarían el injerto de HSPC en esta situación, disminuirían el tiempo de aplasia y eliminarían las restricciones impuestas por la farmacocinética de los fármacos.
Además, más del 80% de los tumores del estroma gastrointestinal, el cáncer colorrectal, el carcinoma de pulmón de células pequeñas y el melanoma se han asociado con mutaciones KIT. En teoría, el trasplante autólogo de HSPC diseñadas podría hacer que las terapias dirigidas por KIT para los cánceres que no se originan en la sangre sean más efectivas.
En conclusión, la edición de epítopos de HSPC puede permitir inmunoterapias más seguras y efectivas cuando las toxicidades dentro del objetivo o fuera del tumor son los factores limitantes clave para una traducción clínica exitosa.
https://www.genengnews.com/topics/translational-medicine/base-editing-tweaks-hsc-epitopes-for-targeted-immunotherapy/
Nuevos PAPELES , PARA LA SALUD .
HEPATITIS A ✅
🦠 HEPATITIS A: La infección viral olvidada que sigue presente
La hepatitis A es una enfermedad infecciosa causada por el virus de la hepatitis A (VHA), un picornavirus altamente resistente al ambiente. Se transmite principalmente por vía fecal-oral, a través de agua o alimentos contaminados. Aunque es prevenible, sigue siendo un problema de salud pública en regiones con malas condiciones sanitarias.
⚠️ ¿Qué síntomas produce?
Tras un período de incubación de 15 a 50 días, los síntomas incluyen:
Fiebre leve
Malestar general
Náuseas y vómitos
Ictericia (coloración amarilla de piel y mucosas)
Orina oscura y heces claras
En muchos casos en niños puede cursar de forma asintomática, pero en adultos jóvenes puede generar cuadros intensos de hepatitis aguda.
🧪 ¿Qué vemos en los análisis?
En sangre, se detecta:
Elevación de transaminasas (ALT y AST > 1000 UI/L)
Bilirrubina elevada
Presencia de IgM anti-VHA, marcador diagnóstico específico
🔬 ¿Por qué importa?
Aunque suele ser autolimitada, puede producir hepatitis fulminante en casos raros. La prevención con vacunas y el acceso a agua segura son claves para su control global.
✅ Prevención inteligente:
Vacuna anti-VHA (2 dosis)
Higiene de manos y alimentos
Educación sanitaria en zonas de riesgo
🔬 Texto revisado por Bioq. Dr. Martin White – Revista A Futura Biotech
NEUROFOTONICA
🧠🎙️ Relato para Video Científico - “Conexiones Cuánticas Infrarrojas
> 🌌 Bienvenidos a A ✅ Futura Biotech, donde la ciencia y la tecnología se entrelazan en los confines del conocimiento.
---
🔹 1. Redes Cuánticas Invisibles
🎙️ "¿Sabías que la información puede entrelazarse a nivel cuántico sin importar la distancia?
Gracias al entrelazamiento cuántico, dos o más partículas pueden vincularse tan profundamente que lo que ocurre en una afecta instantáneamente a la otra... incluso si están separadas por años luz.
Hoy, los científicos exploran la luz infrarroja como portadora de esta información delicada.
¿Por qué infrarrojo? Porque su longitud de onda más larga viaja lejos, con mínima pérdida.
Esto abre la puerta a una Internet cuántica ultra-segura y sensores distribuidos a nivel global."
---
🔹 2. Neuronas con Interconexión Infrarroja Cuántica
🎙️ "Imagina un cerebro donde las neuronas no solo se conectan con neurotransmisores... sino también con luz."
Una teoría emergente sugiere que campos infrarrojos cuánticos podrían permitir a las neuronas comunicarse a velocidades ultrarrápidas.
Este tipo de conexión no-local podría reconfigurar nuestra visión sobre la conciencia, la cognición y las enfermedades neurológicas.
Estudios en biofotónica y coherencia cuántica ya comienzan a respaldar esta hipótesis.
El futuro del cerebro podría ser más cuántico de lo que pensamos.
🔹 3. La Conexión Infrarroja es Cuántica
🎙️ "Cada vez que haces clic en un control remoto… estás usando física cuántica."
Aunque lo percibimos como algo clásico, la conexión infrarroja se basa en el intercambio de fotones discretos de energía, un concepto clave en mecánica cuántica.
Los LEDs emiten fotones infrarrojos cuando los electrones caen de niveles energéticos.
Estos fotones son detectados y transformados en datos.
Detrás de cada dispositivo cotidiano, hay una danza cuántica invisible.
🔹 4. El Infrarrojo y la Materia Cuántica
🎙️ "¿Qué secretos cuánticos esconde la luz infrarroja?"
Los fotones infrarrojos tienen la energía ideal para excitar transiciones vibracionales y rotacionales en moléculas.
Esto permite estudiar materiales sin destruirlos, analizar compuestos con precisión o incluso controlar procesos biológicos.
Desde la espectroscopía de alta precisión, hasta la computación cuántica…
El infrarrojo es una ventana hacia las profundidades invisibles de la materia.
Cierre
> 💡 "Estamos entrando en una nueva era, donde la luz, la mente y la materia se conectan en redes invisibles de pura información cuántica.
Desde la sinapsis hasta el cosmos, el infrarrojo cuántico podría ser el nuevo lenguaje del universo."
📢 Seguí explorando el futuro en A ✅ Futura Biotech – Tu punto de partida para la ciencia que viene.